近日,FDA加速审批RET抑制剂“普拉替尼”上市。这是FDA批准的第二个RET抑制剂,也是首个拥有NGS伴随诊断产品的RET抑制剂。
2020年,FDA加速审批了两个RET抑制剂,RET突变对于癌症临床的意义大幅提升,检测RET突变对于患者更有可能获益。
2020年5月8日,FDA依据LIBRETTO-001 1/2期临床试验结果加速批准首个RET抑制剂:Loxo Oncology 公司的selpercatinib(LOXO-292,商品名:Retevmo)上市,用于治疗RET融合NSCLC,RET突变甲状腺髓样癌(MTC)和RET融合其他类型甲状腺癌(TC)患者。2020年9月4日,FDA依据 ARROW 1/2期临床试验结果加速批准 Blueprint Medicines 公司的RET抑制剂 pralsetinib(普拉替尼,BLU-667,商品名:Gavreto)上市,用于治疗RET融合的非小细胞肺癌(NSCLC)成人患者。
RET基因是个原癌基因,全称是:REarranged during Transfection(转染重排)。RET激活融合和突变是许多癌症类型(包括NSCLC和多种类型的甲状腺癌)的关键致病驱动因素。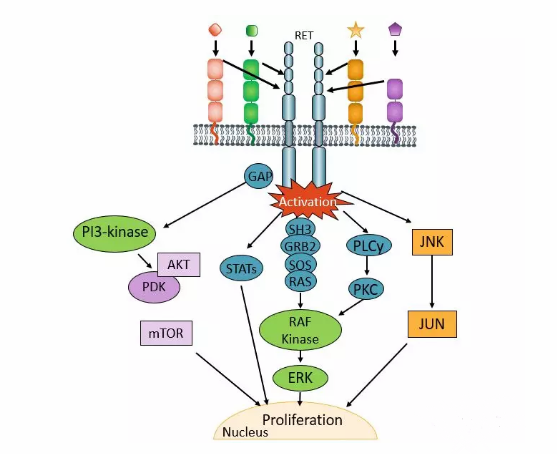
约1~2%的NSCLC(RET重排常见于非吸烟者或曾轻度吸烟者,年龄小于60岁,腺癌、早期淋巴结转移和晚期NSCLC患者中)和10~20%的乳头状甲状腺癌会出现RET融合突变,约90%的晚期甲状腺髓样癌会出现RET突变,另外,在结肠直肠癌,乳腺癌,胰腺癌和其他癌症以及具有治疗耐药性EGFR突变的NSCLC患者中,也会观察到低频的致癌性RET融合。
此前RET突变检测常用于指导卡博替尼、凡德他尼的选择和使用。但卡博替尼、凡德他尼不仅抑制RET蛋白信号,同时会抑制VEGFR、EGFR等其他蛋白。
今年FDA新批的Retevmo、普拉替尼都属于高选择性RET抑制剂,只抑制RET蛋白信号,更精准且毒副作用更小。
RET检测推荐使用NGS方法
RET变异检测方法建议首选 DNA/RNA-base NGS,其次是FISH或RT-qPCR,IHC不推荐使用。
RET常见检测方法对比
此次普拉替尼获批,同步获批的伴随诊断产品使用的也是NGS方法,伯豪医学伯朗康12、伯朗康24及伯靶康等panel检测RET基因重排/融合是基于RNA-based NGS方法,结果更直接准确,也更受认可。
对于想要尝试RET抑制剂的患者,伯豪医学检验提供荧光原位杂交(FISH)平台单项检测项目服务,也提供多个NGS检测项目服务方案,以适应不同的临床需求:
肿瘤个体化单项(FISH):
RET基因重排分析
肿瘤多基因平行检测panel(NGS):
伯朗康/益12-肺癌靶向12基因-多基因药物评估
伯朗康/益24-肺癌靶向24基因-多基因药物评估
伯靶康-精准实体瘤52基因-多基因药物评估
伯百康/益-精准肿瘤118基因-多基因药物评估
伯全康/益-精准肿瘤560基因-多基因药物评估
伯豪医学检验在生命科学和健康领域提供精准的医学实验室服务,服务项目涵盖疾病风险评估 、早期筛查、诊断、个体化医疗、疗效评估、复发监控的全过程分子检测。
1.https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pralsetinib-lung-cancer-ret-gene-fusions2.RET抑制剂丨FDA批准第二个RET抑制剂『普拉替尼』上市,NGS成伴随诊断方法!



