恩曲替尼获国内临床试验许可,伯豪医学多项目助患者寻生机
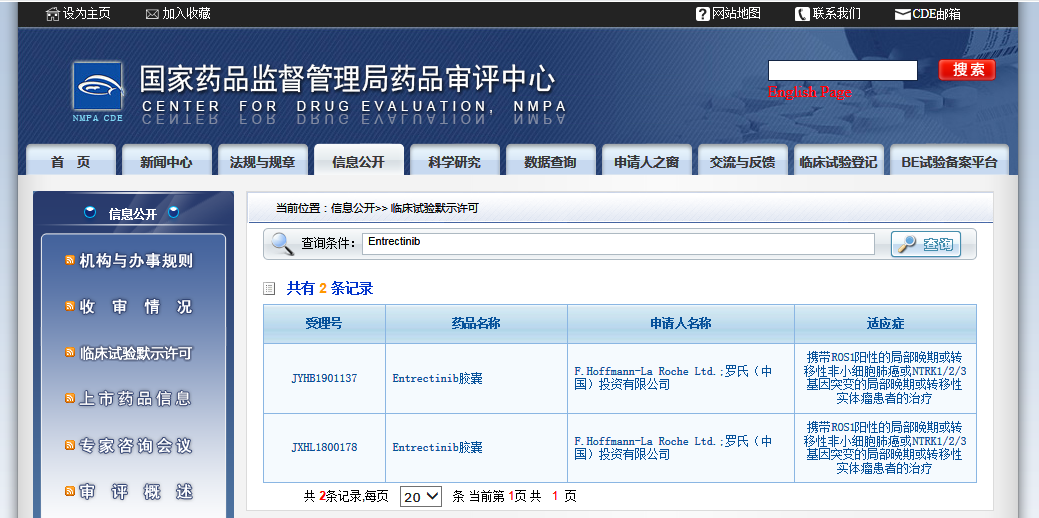
近日,罗氏(中国)的抗癌新药恩曲替尼(商品名:Rozlytrek,通用名:Entrectinib)获得国家药品监督管理局药品评审中心“临床试验默示许可”,用于治疗“携带ROS1阳性的局部晚期或转移性非小细胞肺癌或NTRK1/2/3基因突变的局部晚期或转移性实体瘤患者的治疗”。
恩曲替尼是FDA批准的第二款靶向NTRK融合的精准疗法,也是第三款“不限癌种”疗法(相关药物见文章末尾拓展信息),并且可以通过血脑屏障,为患者带来了更多希望。
FDA的批准是基于关键的Ⅱ期临床试验STARTRK-2、I期研究STARTRK-1、I期研究ALKA-372-001,以及在儿童患者中开展的I/II期STARTRK-NG研究的一系列临床试验的数据。
实验数据显示,恩曲替尼的总体客观缓解率高达57%~78%且耐受性良好,有的患者肿瘤病灶完全消失,对于脑转移的患者也有很好的效果。(具体数据见文章末尾拓展信息)
适用人群
1、 通过基因检测发现NTRK融合阳性的成人实体瘤患者
2、 通过基因检测发现ROS1阳性的局部晚期或转移性非小细胞肺癌患者
伯豪医学适用的检测项目
单项(FISH)
NTRK1基因重排分析
ROS1基因重排分析
套餐(NGS)
伯朗康12
-肺癌靶向12基因-FFPE多基因药物评估 含NTRK1、ROS1基因重排
伯朗益12
-肺癌靶向12基因-cfTNA多基因药物评估 含ROS1基因重排
伯朗康24
-肺癌靶向24基因-FFPE多基因药物评估 含NTRK1、ROS1基因重排
伯朗益24
-肺癌靶向24基因-ctDNA多基因药物评估 含NTRK1~3、ROS1基因重排
伯百康
-精准肿瘤118基因-FFPE多基因药物评估 含NTRK1~3、ROS1基因重排
伯全康
-精准肿瘤560基因-FFPE多基因药物评估 含NTRK1~3、ROS1基因重排
1、FDA批准的不限癌种的三种药物:
帕博丽珠单抗(商品名:Keytruda,通用名:pembrolizumab):用于MSI-H或者dMMR类型的多种实体瘤
拉罗替尼(商品名:Vitrakvi,通用名:larotrectinib):用于NTRK基因融合的多种实体瘤
恩曲替尼(商品名:Rozlytrek,通用名:Entrectinib):用于NTRK基因融合的多种实体瘤
https://zhuanlan.zhihu.com/p/78651661
http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=25
https://www.fda.gov/news-events/press-announcements/fda-approves-third-oncology-drug-targets-key-genetic-driver-cancer-rather-specific-type-tumor

